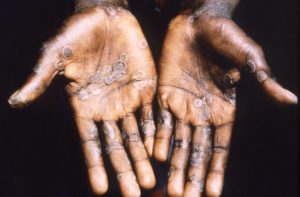
Piden proteger mascotas tras publicación del primer contagio animal-hombre de la viruela del mono
Tras la publicación del primer caso mundial de contagio animal-hombre de la viruela del mono, específicamente en la ciudad de París, Francia, y según lo